Pixabay License Freie kommerzielle Nutzung
Kein Bildnachweis nötig
Baby lass uns impfen..
ich und Du wir zwei…
Du kannst mir vertrauen…
Wer nicht Werbevideos vertraut , die tanzende Menschen zeigen die Ihre Freiheit wieder bekommen sollte sich die folgenden Unterlagen ansehen.
Im Besonderen sollten Sie sich anschauen, wie die Einschätzung des Paul Ehrlich Institutes im Zeitraum von nicht einmal 7 Wochen geändert hat :
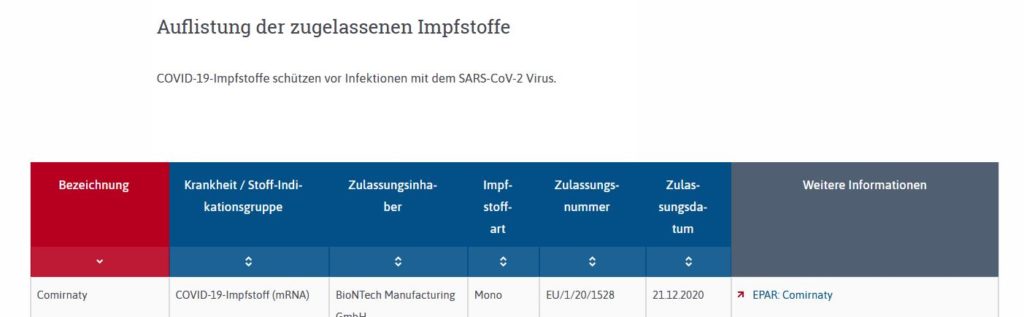

Am 15.08.2021 schützten die Impfstoffe noch vor Infektionen mit dem Sars-CoV-2 Virus.
Am 07.09.2021 schützten die Impfstoffe nur noch vor einem schweren Verlauf einer Infektion mit dem Sars-CoV-2 Virus.
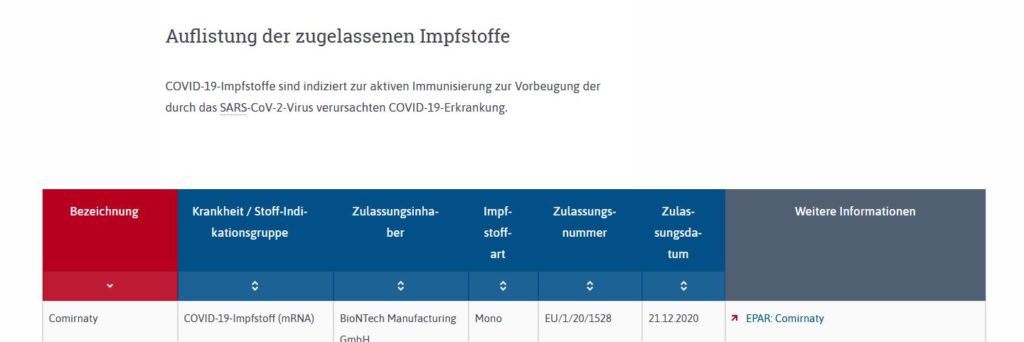
Seit Oktober 2021 sind die Impfstoffe indiziert zur aktiven Imunisierung zur Vorbeugung der durch SARS-Co-V2 verursachten COVID 19 Erkrankung.
Dies bedeutet im Klartext das keine Schutzwirkung des Impfstoffes mehr angegeben wird.
Der Impfstoff kann wirken, muss es aber nicht.
Mit Datum des 23.08.2021 hat die FDA den Impfstoff Comirnaty der Pfizer Biontech Manufacturing GmbH in den USA zugelassen.
Die FDA–Zulassung für Lebensmittel geht zurück auf die „Food and Drug Administration“. Dabei handelt es sich um eine wohlgemerkt US-amerikanische Behörde, der unter anderem die Marktüberwachung von Lebensmitteln, Medikamenten und Medizinprodukten untersteht.
Was ist die FDA?
Die FDA-Zulassung für Lebensmittel geht zurück auf die „Food and Drug Administration“. Dabei handelt es sich um eine wohlgemerkt US-amerikanische Behörde, der unter anderem die Marktüberwachung von Lebensmitteln, Medikamenten und Medizinprodukten untersteht. Vergleichbar ist die Behörde damit in etwa mit einer Kombination aus der deutschen Lebensmittelüberwachung, sowie Teilen der Gewerbeaufsichts- und Gesundheitsämter.
Keiner der gegenwärtig verabreichten Impfstoffe hat eine reguläre Zulassung.
Für Europa wird das Zulassungsverfahren für COVID-19-Impfstoffe durch die Europäische Arzneimittelagentur EMA (European Medicines Agency) koordiniert. Die Impfstoffbewertung der EMA nehmen die Expertinnen und Experten der nationalen Arzneimittelbehörden Europas vor. Erfüllt der Impfstoff alle Bedingungen und überwiegt sein individueller und sein Public Health-Nutzen gegenüber seinen Risiken, wird nach erfolgreichem Zulassungsverfahren von mehreren Monaten eine Zulassungsempfehlung an die Europäische Kommission gegeben, die die Zulassung erteilt. Danach kann der Impfstoff vermarktet und am Menschen angewendet werden. Eine Empfehlung für das Impfen gegen eine Infektionskrankheit gibt in Deutschland die Ständige Impfkommission (STIKO) beim Robert-Koch-Institut (RKI), in der das Paul-Ehrlich-Institut (PEI) als Gast vertreten ist.
Comirnaty /Pfizer Biontech Manufacturing GmbH
Verwendung ab einem Lebensalter von 12 Jahren / Use from 12 years of age onwards
COVID-19 Vaccine Janssen
Spikevax (COVID-19 Vaccine Moderna)
Vaxzevria (COVID-19 Vaccine AstraZeneca)